自由基疗法是肿瘤治疗的重要研究方向,光动力疗法等传统自由基治疗手段的作用机制高度依赖氧气,而实体肿瘤内部普遍存在的乏氧微环境,使其对深部肿瘤、转移瘤的治疗效果大打折扣。电动力疗法(EDT)可通过电场刺激产生自由基,全程不依赖氧气,成为攻克肿瘤乏氧难题的潜在方向。但现有研究多基于金属电极或无机材料开展,如何实现该疗法的精准靶向,并有效激活后续抗肿瘤免疫应答,是领域内亟待突破的关键科学问题。近日,西北工业大学柔性电子研究院黄维院士团队李鹏教授、贾庆岩副教授团队在化学领域国际顶级期刊《美国化学会志》(Journal of the American Chemical Society, JACS)发表题为“Electroacupuncture Activated Mitochondria-targeted Polymeric Radicals for cGAS-STING-activated Immunotherapy”的研究论文,提出了电针驱动的有机自由基介导电动力疗法与cGAS-STING通路介导免疫疗法协同的肿瘤治疗新策略,为攻克肿瘤乏氧难题、实现精准高效的肿瘤免疫治疗提供了全新解决方案。
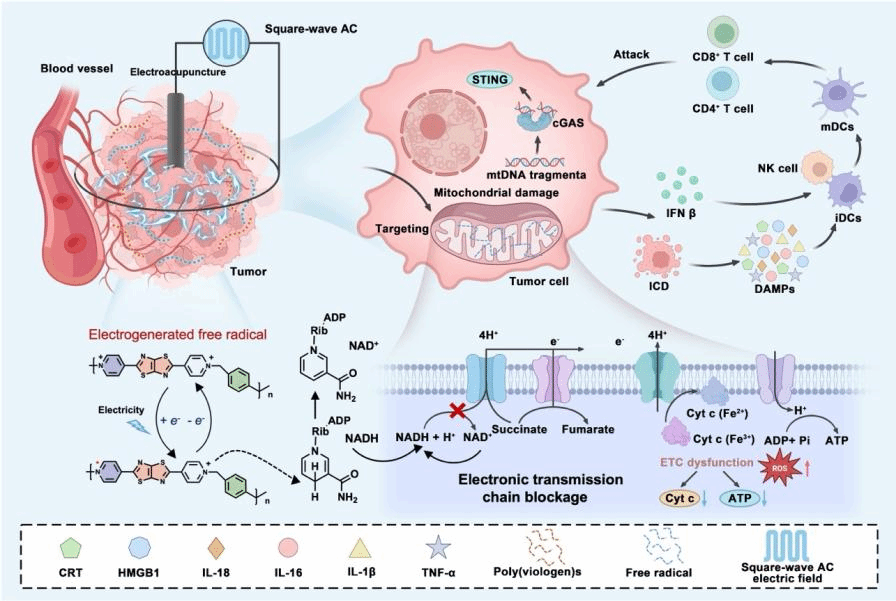
图1. 电针诱导有机自由基生成及其线粒体靶向EDT和cGAS-STING免疫疗法示意图
该研究成功构建了电针驱动的Viologen-EDT平台,实现了对肿瘤细胞线粒体的精准靶向富集。线粒体作为细胞的“能量工厂”,是调控肿瘤细胞生存的关键靶点。研究发现,在特定低频方波交流电的电针刺激下,该平台中的紫精衍生物P(DBPX-TTz-Bpy)可稳定生成有机自由基,且这一过程完全不依赖氧气,从根本上克服了肿瘤乏氧微环境对治疗的限制。
该疗法的抗肿瘤机制呈现双重协同效应:一方面,生成的有机自由基会高效消耗线粒体中的NADH,破坏线粒体电子传递链的正常功能,引发线粒体功能障碍,使肿瘤细胞失去能量供给,同时诱导大量活性氧产生,造成肿瘤细胞内严重的氧化应激损伤,实现对肿瘤细胞的直接杀伤;另一方面,活性氧的大量积累会破坏线粒体嵴的结构完整性,导致线粒体DNA片段释放至细胞质中,进而激活环鸟苷酸-腺苷酸合成酶(cGAS)-干扰素基因刺激因子(STING)通路。该通路的激活可进一步促进I型干扰素的表达,推动树突状细胞成熟,促进CD8⁺T细胞与自然杀伤细胞的增殖及肿瘤浸润,最终启动全身性的抗肿瘤免疫应答。
为验证该策略的治疗效果,研究团队开展了系列动物实验。在模拟肿瘤转移的双侧肿瘤模型中,仅对单侧肿瘤进行治疗,未治疗侧的肿瘤生长抑制率达55.79%,证实其具有显著的远隔抗肿瘤效应。而在长期免疫保护模型中,治愈后的小鼠再次接种肿瘤细胞后,体内记忆T细胞可快速启动免疫应答,有效阻止新肿瘤的生长。上述实验结果充分证明,该电动力疗法可有效激活全身性抗肿瘤免疫应答,为机体赋予长效的免疫保护,实现对肿瘤复发的有效抑制。
结论与展望
本研究开发的Viologen-EDT平台,通过有机自由基介导电动力疗法与 STING通路依赖的免疫疗法的有机整合,实现了对肿瘤的高效抑制,且具备毒性低、靶向性强的优势。该技术策略突破了传统肿瘤治疗的微环境限制,大幅提升了肿瘤治疗的精准性与有效性,为肿瘤治疗提供了临床可行的新方法。未来该平台有望成为手术、放疗、化疗的有效替代或补充疗法,尤其在浅表性肿瘤的临床治疗中展现出重要应用潜力。
西北工业大学柔性电子研究院博士研究生李元滢为本论文的第一作者,西北工业大学黄维院士、李鹏教授,贾庆岩副教授和西北师范大学张云秀副教授为该论文的共同通讯作者。本研究受到国家自然科学基金、陕西省重点项目和陕西省杰出青年科学基金等项目资助。
原文链接:https://doi.org/10.1021/jacs.5c19551
(作者:贾庆岩 图片:贾庆岩 审核:王学文)